杨凯(四川省医疗器械检测中心有源医疗器械检测室,成都 611731)
摘要 目的:通过开展在用医用电气设备电磁兼容性评价研究,提升质量监管手段,保障民众用械安 全,促进医疗器械产业健康发展。
方法:梳理可操作的电磁兼容现场检测项目,提出根据使用范围、频 次、风险等因素选择检测品种,为保证全面、有效评价研究提出了需要采取的措施。
结果与结论:充分 考虑在用医疗器械受到的电磁干扰的影响,尽可能防止出现医疗误诊、报警失灵、意外能量输出等危害 患者或医护人员的情况,探索在用医疗器械电磁兼容性评价研究机制。
关键词: 在用医疗器械;电磁干扰;电磁兼容性;现场测试;评价;措施
中图分类号: R197.39 文献标识码:A 文章编号:1002-7777(2019)01-0079-06 doi:10.16153/j.1002-7777.2019.01.014
Electromagnetic Compatibility Evaluation of In-use Medical Devices
Yang Kai (Active Medical Device Testing Office, Sichuan Testing Center of Medical Devices, Chengdu 611731, China)
Abstract Objective: To carry out the study on the electromagnetic compatibility evaluation of in-use medical devices in order to improve the means of quality supervision, to ensure the safety of medical equipment and to promote the healthy development of medical device industry.
Methods: The operational field test items of electromagnetic compatibility were analyzed, the suggestion that the selection of test varieties should be done according to the scope of use, frequency, risk and other factors was put forward, and the necessary measures to ensure comprehensive and effective evaluation were also proposed.
Results and Conclusion: The effects of electromagnetic interference on inuse medical devices were fully analyzed so as to prevent medical misdiagnosis, alarm failure, unexpected energy output and other hazards to patients or medical staffs and to explore the mechanism of electromagnetic compatibility evaluation of in-use medical devices.
Keywords: in-use medical devices; electromagnetic interference; electromagnetic compatibility; on-site testing; evaluation; measures
1 引言
电磁兼容性[1](Electromagnetic Compatibility,
EMC),是指有源电子设备在其电磁环境中能正常
工作,但不对该环境中任何事物构成不能承受的电
磁骚扰的能力。随着电子设备数量和种类的增加,
电磁辐射呈现指数级增长,已成为继大气污染、水
污染和噪声污染之后的第4大污染[2],特别是医疗
机构中医疗电气设备极易受到电磁干扰的影响,给患者和医护人员造成危害。因此,加强在用医疗器
械电磁兼容性评价研究势在必行。
2 电磁兼容性评价背景
原[敏感词]食品药品监督管理总局于2012年发布的
《关于YY 0505-2012医疗器械行业标准实施有关
工作要求的通知》(食药监办械〔2012〕151号)
要求:第I类和Ⅱ类医用电气设备于2015年1月1日
起、第Ⅲ类医用电气设备于2014年1月1日起,首次申报注册时应提交符合电磁兼容标准要求的检测报
告。但是,由于强制要求时间较短、生产企业设计
考虑不足、上市产品与注册产品差异或减配设计、
企业不具备电磁兼容测试条件无法自行验证等原
因,在用医疗器械仍然存在较大的电磁干扰风险。
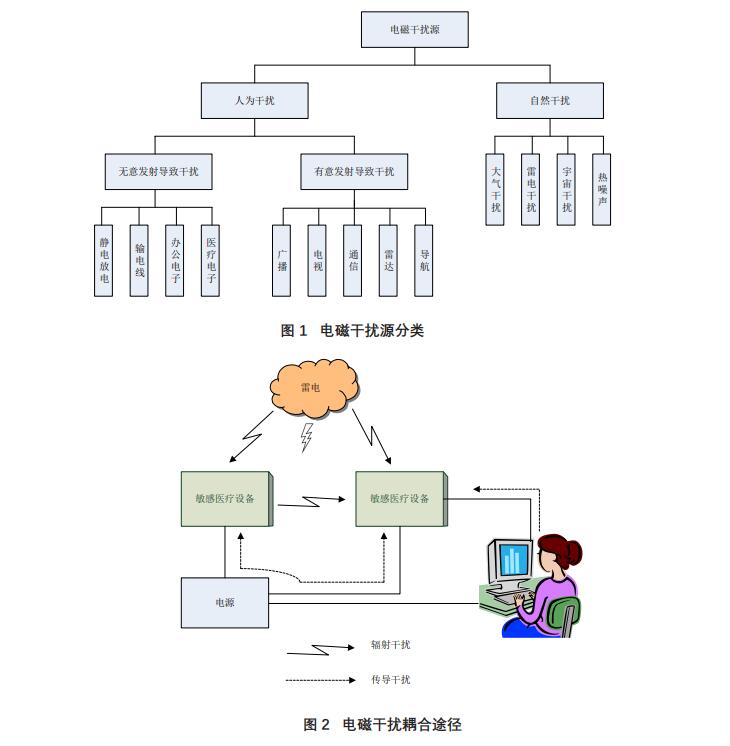
在医疗环境中,干扰源是较为复杂的,如图
1所示。电磁干扰过程中,干扰源通过耦合路径传
输到敏感设备,而任何一个电子设备既可能是干扰
源,又可能是敏感设备,即相互影响,如图2所示。
在电磁环境中,电磁干扰对医疗设备造成的
影响并导致的危害可能会严重影响医疗设备的安全
性和有效性,从而给患者和医疗工作者带来不利的
影响。据国外某权威机构的报告[3]显示:1994年1
月-2005年3月,550份医疗器械不良反应事件中,
可疑是由电磁干扰造成的占70%,其中导致死亡和
致伤的比例占10%。我国也有类似的案例报道,发
现多起医疗事故的罪魁祸首来源于电磁干扰:新生
儿呼吸监护仪等设备出现报警失灵的状况,是因为受到广播电台调制波的影响;某重症病人正在进行
输液抢救的过程中,输液泵出现3次突然中断运转
的现象,调查分析发现,每当附近病人或病人家属
使用手机时,输液泵就会中断工作。
3 电磁兼容性评价项目
为掌握医疗机构在用医疗器械产品质量状
况,发现和化解风险,部分省级监管部门对在用医
疗电气设备开展了监督抽验和评价性抽验工作。
但考虑到现场检验的局限性,这种检验基本上仅验证部分性能指标以及“电压和(或)能量的限
制”“保护接地、功能接地和电位均衡”“连续
漏电流和患者辅助电流”等电气安全通用要求。
四川、陕西、青海、广东等省相继针对高频手术治
疗设备、彩色超声诊断设备、血液分析仪、心电图
机、心电监护仪、中低频治疗仪等开展了抽验工
作。据了解,针对在用医疗器械电磁兼容性检测,
仅北京市开展了传导发射、辐射发射项目的监督抽
验;成都市开展了传导发射、辐射发射、浪涌抗扰
度等项目的评价性抽验,抽验结果不合格率高达60%以上。
医疗器械电磁兼容适用标准主要是YY 0505-
2012和GB/T 18268.1-2010两个基础标准。自强制
检验要求以来,能一次性通过电磁兼容测试的国产
医用电气设备仅占30%左右,超过70%的设备需要
进行整改,而多次反复整改后的产品势必增加成本
投入、结构改变,极可能与上市出售产品不一致。
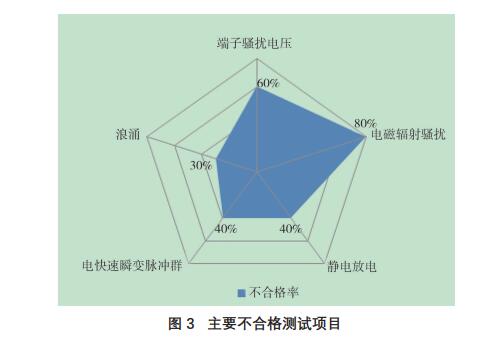
以近50批检测产品为例,不合格项主要集中在图3
所示的几个项目。
针对在用医疗器械评价测试,如果是小型
的、可移动的,可考虑进行实验室测试,测试项
目[敏感词]覆盖图3中的所有项目。但在现场测试,
考虑到测试环境的不确定性和待测电气设备的尺
寸、边界条件等因素,又要尽可能地不耽误其正
常使用。综合医疗不良事件反应案例,可考虑静
电放电(ESD)、电快速瞬变脉冲群(EFT)、浪
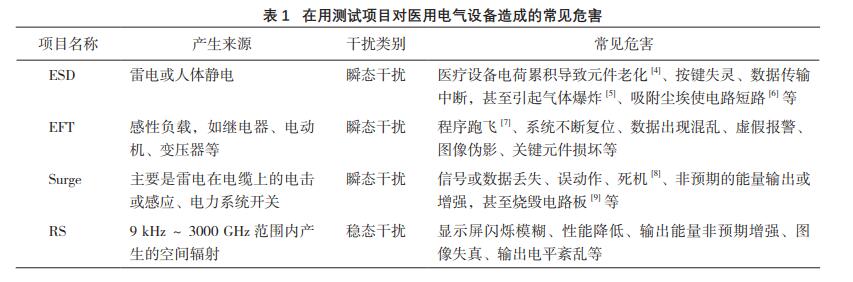
涌(Surge)、射频电磁场辐射(RS)4个项目,以基本验证在用医疗器械的可靠性和有效性,此4个
项目对在用医用电气设备造成的常见危害如表1所
示。当然,ESD、EFT、Surge均属于破坏性实验,
为降低测试过程中对医疗供电网络可能造成的干
扰,条件允许情况下,待测设备[敏感词]单独供电且在
非工作时段测试。同时,为防止测试时引起的空间
辐射对其他敏感设备的影响,测试场地要保证至少
3米的净空间,测试环境要保证合理的温湿度。
其中,射频电磁场辐射抗扰度测试作为电气、
电子设备受到射频电磁场辐射时的性能评定依
据,是医用电气设备电磁兼容抗扰度试验的基本要
求 [10]。特别是医用核磁共振成像(MRI)、大型
X 射线机、PET-CT 等大型设备 [11],需要考究有意
或无意空间辐射抗扰性能,因此射频电磁场辐射
也是在用医疗器械评价研究的一个重要内容。YY
0505-2012[1] 中对射频电磁场辐射的替代测试有较
为明确的规定:在安装现场,利用出现在典型健康
监护环境中的射频源(如无线电话、对讲机和其他
合法的发射机)进行试验。试验使用的频率应是
80 MHz ~ 2.5 GHz 范围中工科医(ISM)设备的使
用频率,即 2.4 ~ 2.5 GHz[12] 的基波频率。
当然,替代试验需要对试验现场周围的射频源
进行研究,以充分评价现场医用电气设备的射频电
磁场辐射抗扰度 [13]。在 80 MHz ~ 2.5 GHz 频段内,可以选用如下的干扰源 [14],在实际测试中,应当
调整射频发射源的功率和距离以提供规定的、合适
的试验电平。
1)无线对讲机[15]:民用对讲机频率范围为
409~410 MHz;业余对讲机为144~146 MHz和
430~440 MHz;专业对讲机的工作频率在甚高频
(VHF)是一部分V高段(148~174 MHz)和V低
段(136~160 MHz),另有一部分是全段(136~
174 MHz)。但在特高频(UHF),大部分是U高
段(450~470 MHz)和U低段(400~430 MHz),
极少数是U全段(400~470 MHz)。
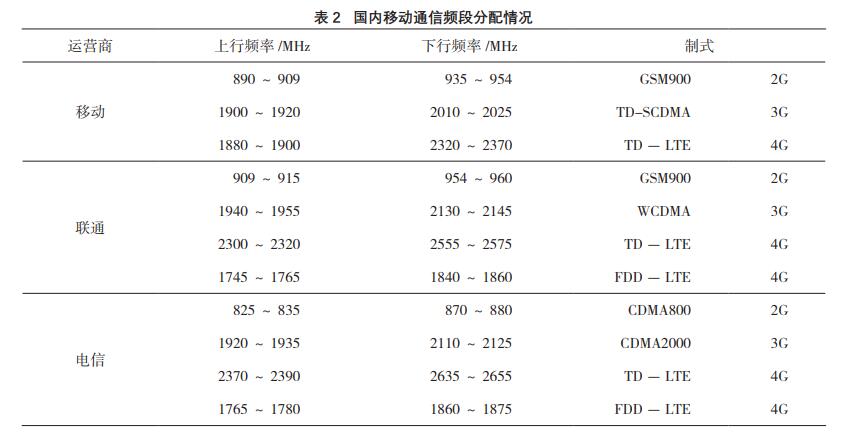
2)移动手机:频率范围如表 2 所示。
3)无线路由器:按照 IEEE 802.11 b/g/n 定义,
工作频率为 2400 ~ 2497MHz。
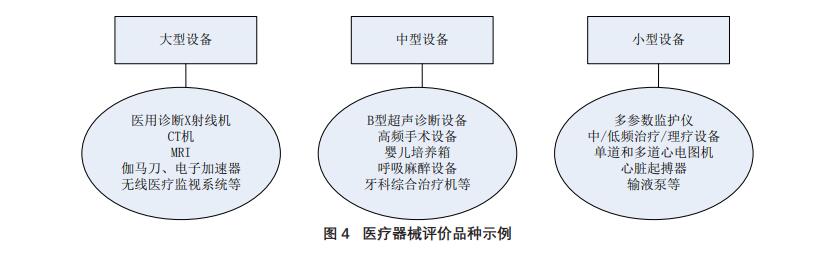
电磁兼容性评价的医疗器械品种可根据使用
频次、范围、风险等因素择机考虑,如图4所示。
4 建议采取的措施
对于重点监管的医疗器械,因其风险高、使
用频繁、体积大等原因,无法抽取样品进行实验室
检测,现场检验便成为对其质量进行监管的主要手段。因此,结合实际工作,需要从以下几个方面采
取措施。
4.1 破解法律法规方面的制约
在用医疗器械检验,特别是电磁兼容检验,
在全世界都是一个新的课题,我国更是刚刚起步,
没有任何成功经验可循[16]。在法律法规层面明确医
疗器械电磁兼容性现场检验的合法性,对现场检验
机构的资质认定、检验方法、检验内容等出具相关
规定,确定根据现场检测结果出具检验报告的法律
地位[17]。2015年12月,广东省食品药品监督管理局
召开《广东省在用医疗器械监督管理办法》立法研
讨会,率先启动在用医疗器械地方立法工作。2017
年2月14日,国务院印发《“十三五”[敏感词]食品安
全规划和“十三五”[敏感词]药品安全规划》(国发
〔2017〕12号),明确提出要“开展在用医疗器械
现场检验方法、检测平台及装备研究”。
4.2 破解设备人员方面的制约
医疗器械电磁兼容性检验属于专业性较强的
测试项目,现场检验要求用于检验的设施设备均
是可移动、便携的,从而对测试设备提出了较高
要求。因此,需要统筹考虑在用医疗器械电磁兼容
的检测项目,增加可检医疗器械的品种范围。加
快人员培训,打造一支技术卓越、知识面广的检测
队伍。加强新设备、新技术的投入力度,提高在用
医疗器械电磁兼容性检验质量,以期形成全面、有
效、系统性的覆盖评价。
4.3 破解医疗机构重视程度的制约
医疗机构中设备管理部门承担医疗器械的维
保、养护、正常使用等职责,但因为素质能力、技
术水平的不足,往往不能找出医疗电气设备在正常
使用过程中出现的性能下降、诊断错误等原因,甚
至片面地认为是由设备本身质量、电气元件老化引
起的,对电磁干扰的概念模糊不清。因此,需要医
疗机构决策层、使用管理部门充分认识在用医疗器
械存在的电磁干扰现象和可能引发的不良事故[18],
不断丰富电磁兼容性相关知识储备,提升技能水平
素养,由上至下、由点及面构建医疗机构电磁兼容
安全机制[19]。
5 结语
医疗器械直接或间接地接触人体,与诊疗、
治疗及复健密切相关,在医疗环境中工作时,如果
电磁兼容能力差,将会造成数据失真、医疗误诊、
报警失灵、危险带电、意外能量输出等危害患者或
医护人员的情况。因此,开展在用医疗器械电磁兼
容性评价研究,是保障民众用械安全、促进落后产
品更替、提高企业自主研发能力的重要举措,必将
更好地推动医疗器械产业健康发展。
参考文献:
[1] YY 0505-2012 医用电气设备第1-2部分:安全通用要
求并列标准:电磁兼容 要求和试验[S]. 北京:中国标
准出版社,2013.
[2] 严红剑,徐秀林,胡秀枋,等. 医用电子设备电磁发射
对医疗环境影响的分析[J]. 中国辐射卫生,2007,16
(3):327-329.
[3] 高静. 医疗器械生产企业在通过电磁兼容标准时所遇到
的问题及改进措施[D]. 北京:北京理工大学,2015.
[4] 高虹. 医疗仪器使用中的静电放电的危害及防护[J]. 医
疗设备信息,2002,(9):37-39.
[5] 林蕾,邓微,武颖. 医疗设备的静电综合防护研究[J].
计算机工程与应用,2013,49(S3):507-510.
[6] 孙小立. 浅析医疗仪器的静电[J]. 医疗装备,2014,27
(9):100.
[7] 罗惠敏. 电子产品电快速瞬变脉冲群干扰的防护[J]. 无
锡职业技术学院学报,2011,10(3):43-45.
[8] 兰建斌,黄美萍. 医疗系统的防雷设计方案[J]. 工程技
术,2015,(9):65.
[9] 郭建松. 浪涌电压对电子设备的危害及防护[J]. 电力技
术,2015,(17):155.
[10] GB/T 17626.3-2016 电磁兼容试验和测量技术 射频电
磁场辐射抗扰度试验[S]. 北京:中国标准出版社,
2016.
[11] 王琦,陈以水,陈顺乐. 加强大型医疗设备的性能检测
和监督管理[J]. 中国辐射卫生,2012,21(2):159-
160.
[12] GB 4824-2013 工业、科学和医疗(ISM)射频设备骚
扰特性 限值和测量方法[S]. 北京:中国标准出版社,
2014.
[13] 黄文广,孟志平. 大型医用电气设备的现场射频电磁场
辐射抗扰[J]. 医疗装备,2018,31(5):33-35.
[14] 陈婷,余华通,邹明明,等. 大型医疗设备或系统EMC
现场测试方法研究[J]. 测试与测量,2012,(2):
25-27.
[15] 王权,苏宗文,李澍,等. 大型医用电气设备的电磁兼
容现场测试[J]. 中国医疗设备,2015,30(9):70-
71.
[16] 杨振. 我国《在用医疗器械检验技术要求》编制构想
[J]. 中国药事,2016,30(1):55-58.
[17] 刘秋颖,王颖,刘然,等. 在用医疗器械科学监管的形
势分析及对策[J]. 中国医疗器械信息,2018,(3):151-152.
[18] 李静莉,郑佳,余新华. 在用医疗器械科学监管的形势
分析与建议[J]. 中国医疗设备,2015,30(1):68-
70.
[19] 唐波,涂彧,张殷,等. 医疗行业决策、管理层辐射安
全与安全文化素养的调查研究[J]. 中国辐射卫生,
2012,21(4):410-412.
中国药事 2019 年 1 月 第 33 卷 第 1 期







