《胃管产品注册审查指导原则(2023年修订版)》公开征求意见(附全文)
2023-04-28
刚刚,GJ药品监督管理局医疗器械技术审评中心发布《胃管产品注册审查指导原则(2023年修订版)》,内容如下: 胃管产品注册审查指导原则(2023年修订版) 本指导原则旨在帮助和指导注册申请人对胃管注册申报资料的准备及撰写,同时也为医疗器械技术审评部门对注册申报资料的技术审评提供参考。 本指导原则是对胃……
《医用口罩产品注册审查指导原则(2023年修订版)》公开征求意见(附全文)
2023-04-28
刚刚,GJ药品监督管理局医疗器械技术审评中心发布《医用口罩产品注册审查指导原则(2023年修订版)》,内容如下: 医用口罩产品注册审查指导原则(2023年修订版) 本指导原则旨在指导注册申请人对医用口罩产品注册申报资料的准备及撰写,同时也为技术审评部门对注册申报资料的审评提供参考。 本指导原则是对医用……
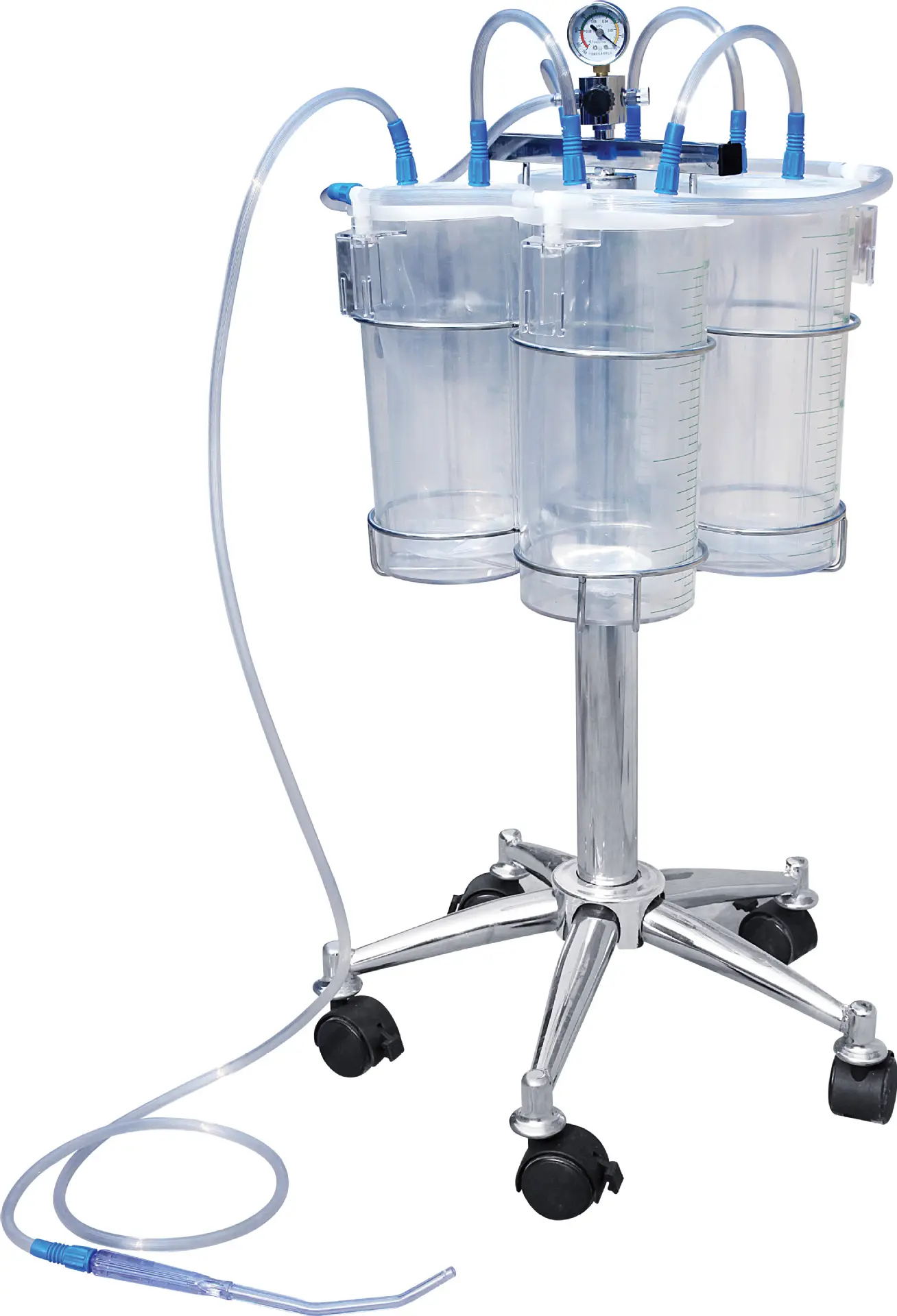
《负压引流装置产品注册审查指导原则(2023年修订版)》公开征求意见(附全文)
2023-04-28
刚刚,GJ药品监督管理局医疗器械技术审评中心发布《负压引流装置产品注册审查指导原则(2023年修订版)》,内容如下: 负压引流装置产品注册审查指导原则(2023年修订版) 本指导原则旨在指导注册申请人对负压引流装置产品注册申报资料的准备及撰写,同时也为技术审评部门提供参考,帮助审评人员理解和掌握该类产品原理……
《义齿制作用合金产品注册审查指导原则(2023年修订版)》公开征求意见(附全文)
2023-04-27
刚刚,GJ药品监督管理局医疗器械技术审评中心发布《义齿制作用合金产品注册审查指导原则(2023年修订版)》,内容如下: 义齿制作用合金产品注册审查指导原则(2023年修订版) 本指导原则旨在指导注册申请人对义齿制作用合金产品注册申报资料的准备及撰写,同时也为技术审评部门对注册申报资料的审评提供参考。 ……
《气管插管产品注册审查指导原则(2023年修订版)》公开征求意见(附全文)
2023-04-27
刚刚,GJ药品监督管理局医疗器械技术审评中心发布《气管插管产品注册审查指导原则(2023年修订版)》,内容如下: 气管插管产品注册审查指导原则(2023年修订版) 本指导原则旨在指导注册申请人对气管插管产品注册申报资料的准备及撰写,同时也为技术审评部门提供参考。 本指导原则是对气管插管……
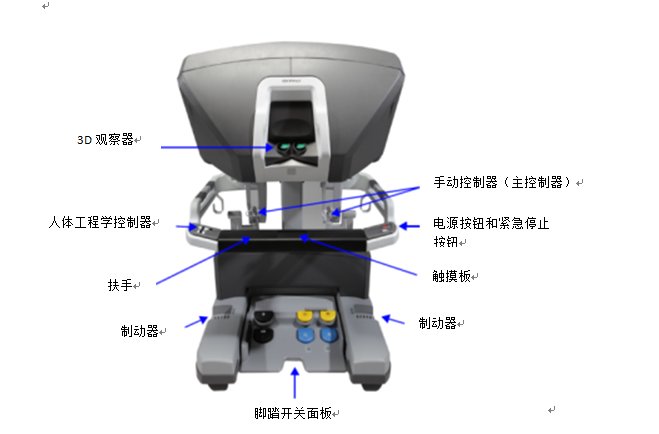
《腹腔内窥镜手术系统临床试验技术审评要点》公开征求意见(附全文)
2023-04-25
刚刚,GJ药品监督管理局医疗器械技术审评中心发布《腹腔内窥镜手术系统临床试验技术审评要点》,内容如下: 腹腔内窥镜手术系统临床试验技术审评要点 本要点旨在指导注册申请人对腹腔内窥镜手术系统开展同品种临床评价,同时也为技术审评部门审评腹腔内窥镜手术系统同品种临床评价资料提供参考。 本要点……
《腹腔内窥镜手术系统技术审评要点(2023年修订版)》公开征求意见(附全文)
2023-04-25
刚刚,GJ药品监督管理局医疗器械技术审评中心发布《腹腔内窥镜手术系统技术审评要点(2023年修订版征求意见稿)》,内容如下: 腹腔内窥镜手术系统技术审评要点 本审评要点旨在指导注册申请人对腹腔内窥镜手术系统产品注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。 本……
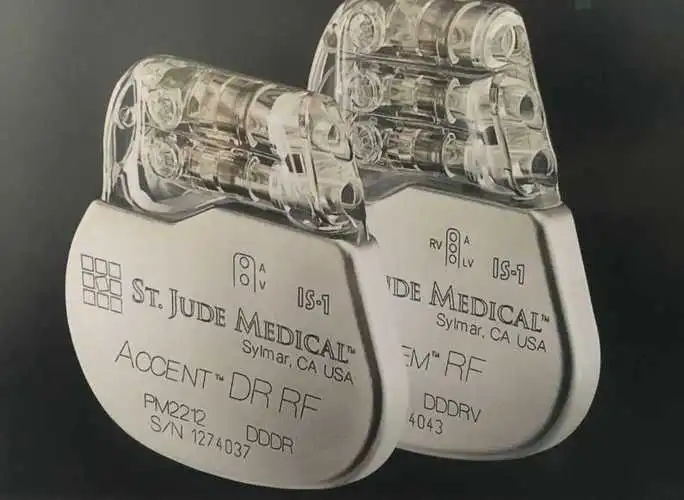
心脏起搏器研发实验要求
2023-04-24
植入式心脏起搏器需要植入人体,属于用于心脏的治理,急救装置类的医用电子仪器设备,属于高风险的医疗器械,其分类编号为6821-1,作为III类有源医疗器械进行管理。 一、植入式心脏起搏相关标准 与植入式心脏起搏器的主要国标和行标有GB 16174.1《心脏起搏器第1部分:植入式……