超声手术设备医疗器械注册所需相关标准以及临床评价路径推荐
2023-02-22
什么是超声手术设备? 超声手术设备是一种医疗器械,利用高频声波的热和机械效应来进行手术操作。它包括超声刀、超声剪、超声凝固器、超声消融器等多种不同类型的设备,可以用于各种不同类型的手术操作,包括肝脏切除、肾脏切除、肺切除、甲状腺切除、乳腺切除等。 超声手术设备通常由以下几个组成部分构成: ……
国家药监局发布第三批实施医疗器械唯一标识的产品目录
2023-02-22
2021年1月1日,9大类69种第三类医疗器械第一批实施医疗器械唯一标识。2022年6月1日,其他第三类医疗器械(含体外诊断试剂)第二批实施医疗器械唯一标识。为进一步贯彻落实《医疗器械监督管理条例》《国务院办公厅关于印发治理高值医用耗材改革方案的通知》和国务院深化医药卫生体制改革有关重点工作任务,决定将部分第二类医疗器……
CMDE有源医械电磁兼容技术答疑汇总
2023-02-21
Q1.有源产品在进行电磁兼容检测时,是否需要连同产品组成中的无源附件一起检测? A.通常电磁兼容检验中使用的设备装置、电缆布局和典型配置中的全部附件应与正常使用时一致。如果经分析判定无源附件与电磁兼容检验无关,则不需要连同该无源附件一起检测。如果测试时为了实现其基本性能必须配合无源附件的情况下,应当配合该无源附件进行检测。 Q2.无线连接的有源医疗器械配件是否需要进行EMC检测?纯物理连接的有源医疗器械配件是否需要进行EMC检测? A.有源医疗器械配件是否进行EM
医疗器械注册电子申报等问题答疑汇总
2023-02-21
为方便企业办理医疗器械电子申报相关业务,市器审中心受理部整理了部分高频问题,涉及现场检查不合格项整改资料报送、电子签章、辅助工具使用等,以一问一答的形式帮助办事人员准确高效地办理相关业务事项。 一、问:医疗器械生产质量管理体系现场检查完毕后,企业的不合格项整改资料及复查申请(如有)如何提交上传? ……
医疗器械临床试验质量控制问题分析与探讨
2023-02-20
引言 医疗器械的安全性和有效性直接关系到人民群众的生命健康,国家高度重视医疗器械的质量安全和创新发展。医疗器械临床试验,是指在符合条件的医疗器械临床试验机构中,对拟申请注册的医疗器械(含体外诊断试剂)在正常使用条件下的安全性和有效性进行确认的过程[1]。医疗器械临床试验是产品研发的关键环节,通过临床试验获……
体外诊断试剂如何进行设计转换
2023-02-20
对于从事医疗器械行业的从业者,对于“设计转换”一词应该不陌生,中国医疗器械生产质量管理规范和ISO 13485都对“设计转换”提出了要求。 1、什么是设计转换? 设计转换是指从医疗器械样品试制、小批量试产、中试到实现质量稳定地、持续有序地批量化、规模化生产的过程。狭义的转换可以浅显理解为“转……
一次性内镜下耗材活检钳手柄结构注意要点
2023-02-20
一次性内窥镜低成本、耗材化,可进行专用性的的产品集成和创新迭代,迸发出巨大的临床应用想象空间和商业化潜能,有望成为颠覆医用内窥镜市场的新一代技术变革! 本文将围绕一次性内镜下耗材如活检钳、旋转闭合夹等,本文主要介绍活检钳手柄结构有哪些注意要点。 一、芯杆直线度……
我国消毒产品领域标准化现状研究
2023-02-17
(一)国家标准研制情况 国家卫生健康标准委员会秘书处设立在国家卫生和健康委员会,下设21个专业委员会。国家卫生健康标准委员会消毒标准专业委员会于1996年成立,目前已是第八届,秘书处设立在中国疾病预防控制中心环境与健康相关产品安全所。国家消毒标委会成立之后,立即组织全国专家开展了十余项国家标准的制订工作。……
有源手术器械相关技术指导原则、标准、临床评价路径汇总
2023-02-17
近日,CMDE官方网站将各类医疗器械、体外诊断试剂的指导原则、标准与临床评价路径重新分类整理,并以列表形式展示。 有源手术器械 一、超声手术设备及附件 1、超声手术设备 指导原则 1、超声软组织切割止血系统注册技术审查指导原则 2、超声软组织切割止血系……
欧洲药典兔热原检查新策略以及与中国药典的对比
2023-02-16
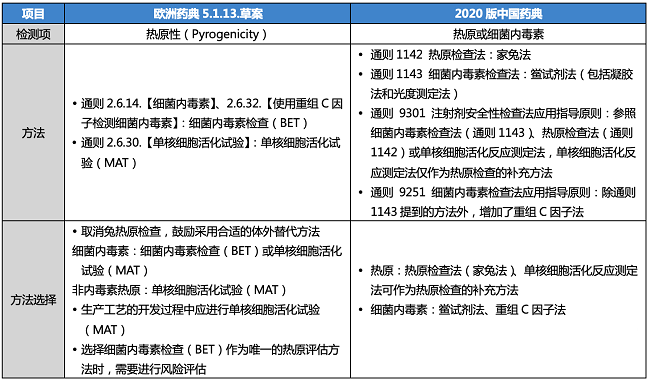
近日,欧洲药典(Ph. Eur.)在药典论坛(Pharmeuropa)35.1中公布了关于兔热原检查(Rabbit Pyrogen Test,RPT)替代策略相关的59篇草案,包括新增通则5.1.13.【热原性(Pyrogenicity)】以及修订其他58个文本,这些文本涵盖了多种产品,包括人用疫苗、血液制品、抗生素、……
GE医疗一级召回核医学600/800系列系统
2023-02-16
GE HealthCare召回核医学600/800系列系统,以防探测器坠落可能伤害患者。FDA认定这是一类召回,是最严重的召回类型。使用这些设备可能导致严重伤害或死亡。 召回产品 产品名称:核医学600/800系列系统 产品型号: 布里沃615 Discovery NM 630 Optima 640 Discovery NM/CT:670 DR、670 ES、670 Pro、670 CZT 纳米:830、830秒 NM/CT:850、8