我国医疗器械监管政策1月起全面调整
2023-02-02
2023年1月1日起,《国家药监局综合司关于加强医疗器械生产经营分级监管工作的指导意见》(以下简称《指导意见》)开始施行。文件将指导各地药品监管部门在医疗器械注册人制度下开展医疗器械生产经营监管工作。 《指导意见》提出了对医疗器械生产经营企业的监管级别划分原则和检查要求,药品监管部门可以按照风险将医疗器械……
2022年医疗器械问答汇总
2023-01-30
Q1. 与免临床目录描述不一致,还可以免临床吗? 免临床目录中的产品如白介素检测试剂,目录用途描述为“用于检测人体样本中的白介素,主要用于监测机体的免疫状态、炎症反应等。”,白介素种类较多,其中产品声称符合上述用途的各种白介素检测项目均可作为免临床产品进行申报,若产品有新的预期用途,如用于特定病原体感染的辅助诊断等用途则不属于
YY/T 1837-2022《医用电气设备 可靠性通用要求》高清下载
2023-01-29
医用电气设备可靠性通用要求 1、范围 本文件规定了医用电气设备(以下简称 ME 设备)和医用电气系统(以下简称 ME 系统)生命周期内开展可靠性工作的通用要求和基本方法。 本文件适用于各类ME 设备或 ME 系统的可靠性工作。本文件不包含专门针对软件可靠性的相关要求和方法。 注:本文件正文中所有……
检定螺旋CT剂量指数(CTDI)应注意的问题
2023-01-29
一、检定螺旋CT剂量指数(CTDI)的设备及检定方法 1.检定设备 采用瑞典RTI辐射测量公司Barracuda X射线机多功能质量检测仪和CT剂量检测模体测量螺旋CT剂量指数。长杆电离室DCT10有效长度为10cm,CT剂量检测模体分为头部模体和腹部模体,由均匀的有机玻璃组成。在模体的中心和近表层位置分布……
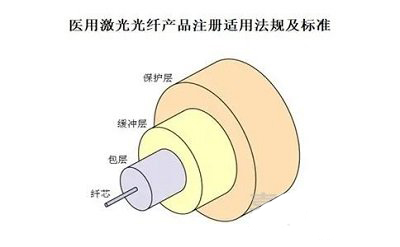
医用激光光纤产品技术要求、注册分类与与相关标准
2023-01-29
医用激光光纤产品通常由光纤、激光器连接接口和手持部组成,用于传输激光能量,在我国属于第二类医疗器械注册产品,在临床上广泛应用。本文为大家整理了医用激光光纤产品注册适用法规及标准。 一、医用激光光纤产品注册适用法规及标准 1.医用激光光纤产品注册技术审查……
中医医疗器械设备标准及对应技术指标
2023-01-29
一、中医器械标准 中医器械是指在诊疗活动中,在中医理论指导下应用的仪器、设备、器具、材料及其他物品(包括所需软件)。 二、中医器械工作原理 中医诊断设备 脉诊设备通常由主机、加压装置和压力传感器组成,经压力传感器,通过皮表对桡动脉及周边组织的腕部寸、关、尺部位,以……
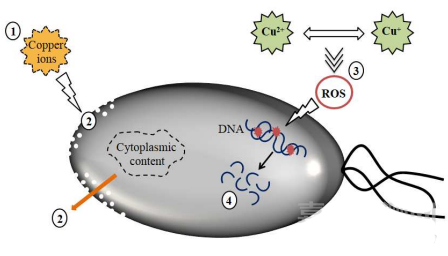
医用金属铜的抗菌性与安全性探究
2023-01-27
近年来,以进一步提高医用金属材料的生物相容性、力学相容性甚至生物活性等为目标的研究和开发方兴未艾,发展出众多新型医用金属材料及相关表面改性技术,为金属医疗器械产品的发展和应用带来了新的机遇。 与人体植入物相关的感染是医学临床中长期存在并迫切需要解决的一个重要问题。在骨科临床中,即使是在严格执行无菌手术操作……
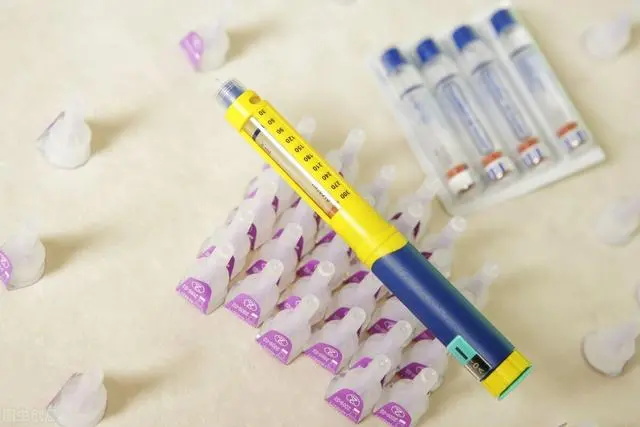
一次性使用注射笔配套用针研发实验要求与主要风险
2023-01-27
注射笔配套用针是指与注射笔配套使用的注射针产品,无菌提供,一次性使用,通常由外护套、内护套、针管、针座、密封透析纸(密封贴膜)组成,其中外护套与密封透析纸(密封贴膜)共同组成产品的初包装。针管一般为双头针头,常用于药物皮下注射。 该产品按照第三类医疗器械管理,属于《医疗器械分类目录》(总局关于发布医疗器械分类目录……