正电子发射/X射线计算机断层成像系统同品种临床评价注册审查指导原则(征求意见稿)
2022-10-25
正电子发射/X射线计算机断层成像系统同品种临床评价注册审查指导原则(征求意见稿) 本指导原则旨在指导注册申请人对正电子发射/X射线计算机断层成像系统(下文简称PET/CT)开展同品种临床评价,同时也为技术审评部门审评PET/CT同品种临床评价资料提供参考。本指导原则是对2020年发布《正电子发射/X射线计……
椎间融合器同品种临床评价注册审查指导原则(征求意见稿)
2022-10-25
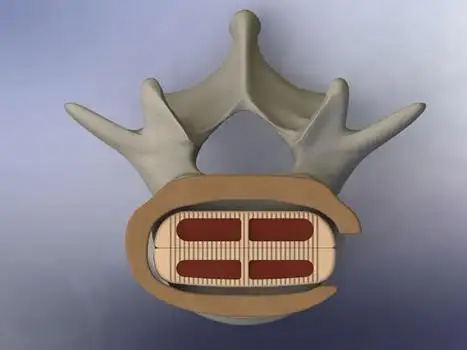
椎间融合器同品种临床评价注册审查指导原则(征求意见稿) 本指导原则旨在指导注册申请人对椎间融合器开展同品种临床评价,同时也为技术审评部门审评椎间融合器同品种临床评价资料提供参考。 本指导原则是对椎间融合器同品种临床评价的一般要求,申请人需依据产品的具体特性确定其中内容是否适用。若不适用,需具体阐述理……
髋关节假体同品种临床评价注册审查指导原则(征求意见稿)
2022-10-25
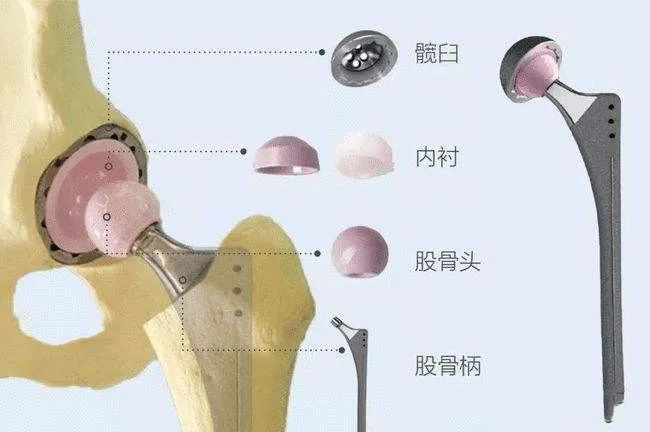
髋关节假体同品种临床评价注册审查指导原则(征求意见稿) 本指导原则旨在指导注册申请人对髋关节假体开展同品种临床评价,同时也为技术审评部门审评髋关节假体同品种临床评价资料提供参考。 本指导原则是对髋关节假体同品种临床评价的一般要求,申请人需依据产品的具体特性确定其中内容是否适用。若不适用,需具体阐述理……
超声软组织手术设备注册审查指导原则
2022-10-25
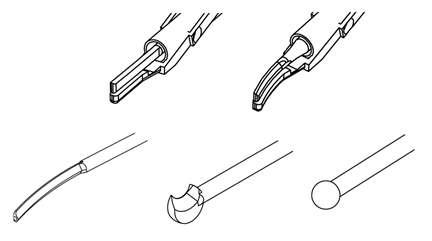
超声软组织手术设备注册审查指导原则 本指导原则旨在指导注册申请人规范超声软组织手术设备注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。 本指导原则是对超声软组织手术设备的一般要求,申请人应依据产品的具体特性确定其中内容是否适用。若不适用,需具体阐述理由及相应的科学依据,并依据……
浅谈创新型医疗器械企业知识产权保护措施
2022-10-24
近年来,国家对医疗器械创新的支持力度不断加大,推动创新型医疗器械企业的自主创新能力快速提高。高端科技逐步普及成为我国医疗器械行业的重要发展趋势,实现高端科技国产化也逐渐成为医疗器械企业的重要发展目标。知识产权作为无形资产,可为医疗器械企业不断推出的创新成果保驾护航,有利于推动国产化进程加速。 创新型医疗器械企业可……
办理进口医疗器械注册对产品检验要求
2022-10-24
进口医疗器械注册与国产医疗器械注册既有区别又有相同点,关于进口医疗器械注册是否需要检验,检验的要求与国产医疗器械注册检验有无差异,在哪来检验,本文为您介绍。 一、进口医疗器械注册检验说明: 很多人对进口医疗器械注册是否需要在中国境内检测存有疑问,因为进口产品在其生产国或注册国已经检测过了,有国外的检……
什么医疗器械产品可以免于注册检测?
2022-10-24
注册证是进入市场的入场券。在我国,第二、三类医疗器械要投入销售、使用,须先按照《医疗器械注册管理办法》或《体外诊断试剂注册管理办法》的相关规定向食药监部门申请产品注册,取得医疗器械注册批件,从而获得进入市场的资格。 而第二、三类医疗器械产品的注册申请,需生产企业向食药监部门提交相关技术资料,包括注册检验报告、临床……
可吸收再生氧化纤维素止血颗粒医疗器械产品注册技术审评报告
2022-10-19
一、产品概述 (一)产品结构及组成 该产品由型号3013SP即再生氧化纤维素可吸收止血颗粒(预装含装置)和型号3123SPEA即再生氧化纤维素可吸收止血颗粒内窥镜施用导管装置组成。两者均经辐射灭菌,一次性使用。型号3013SP为预装3g经专利工艺压实细纤维制成的止血颗粒的施用装置,用于开放手术;型号31……
血管内超声诊断仪医疗器械产品注册技术审评报告
2022-10-19
一、产品概述 (一)产品结构及组成 产品由成像主机(含推车、显示器、键盘、鼠标)、回撤马达组成。 (二)产品适用范围 产品在医疗机构使用,与本公司生产的一次性使用血管内超声诊断导管(型号:02-6F40-01、02-6F60-01)配合使用,适用于将进行冠脉血管内介入手术的患者,预期用于……
ZEM15台式扫描电镜在司法鉴定行业发挥着不可忽略的作用
2022-10-17
ZEM15台式扫描电镜速度快,信号采集带宽10M,可以在视频模式下流畅实时地显示样品。只需鼠标就可完成所有操作,不需对中光阑等复杂步骤,聚焦消像散后可直接拍图,主机集成高压及控制系统,体积小巧,便于移动,安装无需特殊环境,只需找一张桌子,操作简单快捷,维护方便,在硅藻鉴定、纤维鉴定、火灾后物证鉴定中发挥重要作用。 ZEM15台式扫描电镜在司法鉴定行业发挥着不可忽略的作用,它具有检测快速简便,取材少,无损检测,放大倍数高等一系列优点,成为刑事技术检测的重要工具。 1、在火
在台式扫描电镜的基本操作中,如何调整焦距和巧妙地消除像散?
2022-10-17
台式扫描电镜的基本操作包括调整焦距和巧妙地消除像散,想要使用扫描电镜照射出清晰的图像,就需要熟悉sem扫描电镜的各种基本操作及基本要求。 台式扫描电镜基本操作包括调整焦距和巧妙地消除像散。对焦比较容易,改变焦距直到图像清晰。当离焦量较大时,可采用较高的灵敏度,并可在焦点附近降低灵敏度,以实现准确对焦。散光……
医疗器械境外临床试验数据常见问题答疑
2022-10-13
一、《接受医疗器械境外临床试验数据技术指导原则》出台的目的是什么? 为加强医疗器械产品注册工作的管理,进一步提高注册审查质量,鼓励医疗器械研发创新,发布了《接受医疗器械境外临床试验数据技术指导原则》。 二、《接受医疗器械境外临床试验数据技术指导原则》的意义是什么? 该指导原则的……