《乳房植入体产品注册审查指导原则(2024年修订版)》正式发布(附全文)
2024-10-18
刚刚,G家药监局器审中心发布《乳房植入体产品注册审查指导原则(2024年修订版)》,内容如下: 乳房植入体产品注册审查指导原则(2024年修订版) 本指导原则旨在为药品监管部门对乳房植入体注册申报资料的技术审评提供技术指导,同时也为注册申请人进行乳房植入体的注册申报提供参考。 本指导原……
医疗器械产品稳定性验证有效期与运输条件的深度解析
2024-10-18
在医疗器械行业,产品的稳定性验证是确保其在声明的有效期内维持安全性和有效性的重要环节。有效期验证不仅考验着产品的内在质量,还考量着其对外界环境的适应能力,尤其是运输和储存条件的影响。本文将围绕产品有效期验证与运输条件的关系展开讨论,帮助企业理解如何在验证过程中全面考虑各种因素,确保产品的稳定性和可靠性。 ……
人工智能医疗器械注册指导原则解读
2024-10-15
指导原则的适用范围 1.注册申报:适用于第二类、第三类人工智能独立软件和含有人工智能软件组件的医疗器械(包括体外诊断医疗器械);自研软件的注册申报,现成软件组件参照执行,不适用于外部软件环境。 2.体系核查:可用作人工智能医疗器械的体系核查参考。 主要概念 人工智……
解读GB 1588—2024《医用玻璃体温计》(附标准全文)
2024-10-15
一、标准编号、标准名称 标准编号:GB 1588—2024 标准名称:医用玻璃体温计 发布日期:2024年4月29日 实施日期:2026年5月1日 代替标准:GB1588—2001《玻璃体温计》 二、标准修订背景 我国是医用玻璃体温计最大生产国,很多出口……
《影像型超声诊断设备(第三类)注册审查指导原则(2023年修订版)》正式发布
2024-10-14
刚刚,G家药品监督管理局医疗器械技术审评中心发布《影像型超声诊断设备(第三类)注册审查指导原则(2023年修订版)》,内容如下: 影像型超声诊断设备(第三类)注册审查指导原则(2023年修订版) 本指导原则旨在指导注册申请人对影像型超声诊断设备(第三类)注册申报资料的准备及撰写,同时也为技术审评部门……
医疗器械包装测试常见问题答疑
2024-10-10
以下为正文: 1.【问】G家药监局关于医疗器械包装运输试验是怎么规定的? G家药监局发布的《医疗器械安全和性能基本原则》中明确规定:医疗器械的设计、生产和包装,包括申请人所提供的说明和信息,应确保在按照预期用途使用时,运输和贮存条件(例如:跌落、振动、温度和湿度的波动)不会对医疗器械的特性和性能,包……
《金属缆线/缆索系统注册审查指导原则》正式发布(附全文)
2024-10-10
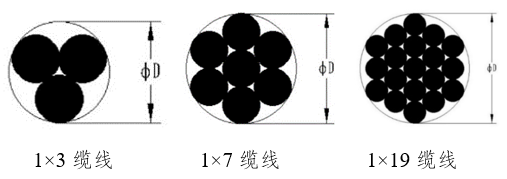
刚刚,G家药品监督管理局医疗器械技术审评中心发布《金属缆线/缆索系统注册审查指导原则》,内容如下: 金属缆线/缆索系统注册审查指导原则 本指导原则旨在指导注册申请人对金属缆线/缆索系统统注册申报资料的准备及撰写,同时也为技术审评部门对注册申报资料的审评提供参考。 本指导原则是对金属缆线……
国家药监局发布34项医疗器械行业标准(附目录)
2024-10-09
G家药监局消息,YY 0271.2—2024《牙科学水基水门汀 第2部分:树脂改性水门汀》等34项医疗器械行业标准已经审定通过,现予以公布。标准编号、名称、适用范围和实施日期如下: 医疗器械行业标准信息表 序号 标准编号
GB 9706.1-2020测试设备参考清单
2024-10-09
新版GB 9706系列标准已于去年5月1日起陆续实施,这一系列标准的关注度也持续不减。此前,中检院公开了全国医用电器标准化技术委员会(SAC/TC10)秘书处联合G家药品监督管理局医用电气设备重点实验室编制的《GB 9706.1-2020测试和测试设备参考清单》,我们将其转载分享给大家。 ……
医疗器械可用性工程注册审查新导则常见问题
2024-10-08
根据G家药品监局器审中心发布的“医疗器械可用性工程注册审查指导原则(2024年第13号)” 自2024年10月8日起,拟提交申请的医疗器械产品根据具体情况提交相应可用性注册申报资料。 1、可用性工程文档与临床试验关系? 答:用户界面确认测试某些关键任务测试项目可能会导致受试者受到严重伤害或死……