无线医用内窥镜技术与专利分析
2022-07-18
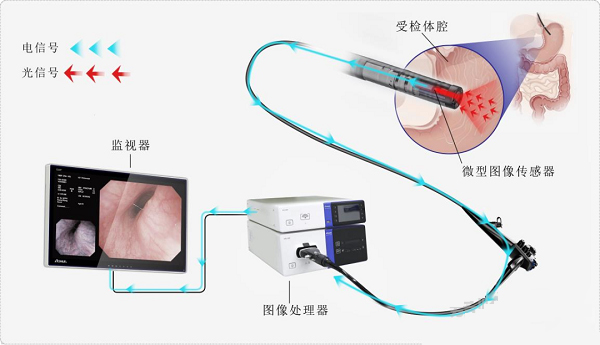
前言导读 医用内窥镜是一种医疗器械,由可弯曲部分、光源及一组镜头组成,用于在内窥镜诊疗过程中提供通道、照明,并可以对体腔、中空器官和身体管道进行观察或操作,其经人体的天然孔道,或者是经手术做的小切口进入人体内。使用时将内窥镜导入预检查的器官,可直接窥视有关部位的变化,亦可用于手术或协助植入治疗性人工产品。……
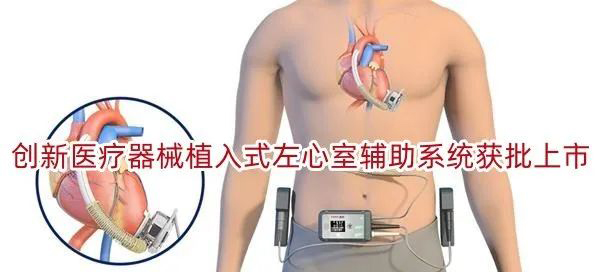
创新医疗器械植入式左心室辅助系统获批上市
2022-07-18
近日,国家药品监督管理局经审查,批准了航天泰心科技有限公司生产的“植入式左心室辅助系统”创新产品注册申请。 该产品由植入部件(血泵、心室缝合环、人造血管保护架)、手术工具(心脏开孔工具、旋紧工具、经皮导线牵引工具、入口管保护帽、手术用经皮导线延长线)、体外部件(控制器、控制器电源延长线、交流电源适配器、锂离子电池……
关于发布医疗器械安全和性能基本原则符合性技术指南的通告
2022-07-15
为构建科学的医疗器械监管体系,加快与国际接轨,2020年3月,我国等同转化IMDRF第三版《医疗器械安全和性能基本原则》(以下简称《基本原则》)。《基本原则》是基于通用风险提炼出的医疗器械安全有效基本要求,注册申请人应自觉履行主体责任,将《基本原则》要求融入医疗器械的研发和生产过程中,在质量管理体系的控制下,形成相应的……
国家药监局:经导管人工肺动脉瓣膜系统获批上市,附已批准创新医疗器械164款
2022-07-14
近日,国家药品监督管理局经审查,批准了杭州启明医疗器械股份有限公司生产的创新产品“经导管人工肺动脉瓣膜系统”注册。 该产品由肺动脉瓣膜和输送系统组成,其中输送系统包括输送导管系统和压缩装载系统。肺动脉瓣膜由自扩张镍钛合金支架、猪心包材质的瓣叶和裙体及缝合线组成。肺动脉瓣膜的设计能够使瓣膜支架锚定更加稳定,适用于不……
国家卫健委:高端医疗装备,有新政策
2022-07-14
医疗器械产业发展已经进入新阶段,越来越多的头部企业和创新企业刺入高附加值市场,国家政策也在持续引导,加强高端医疗器械产业发展。 高端医疗装备,组团研发 7月11日,国家卫健委发布《<高端医疗装备应用示范基地管理办法(试行)>征求意见稿》。《意见稿》指出,根据《“十四五”医疗装备产业发展规……
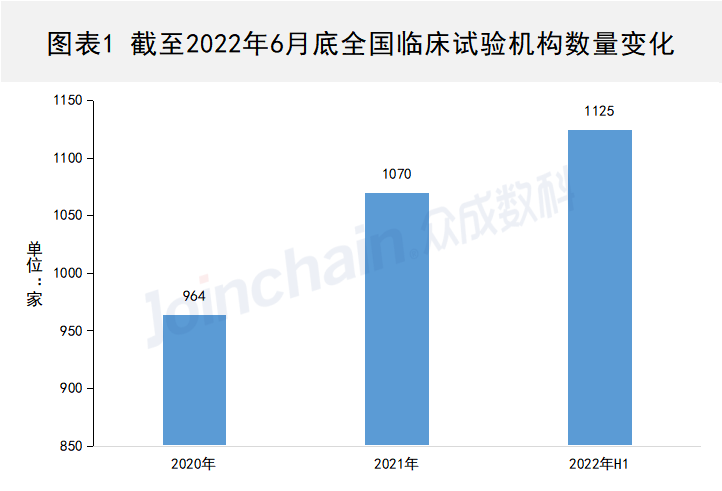
全国临床试验机构数据一览
2022-07-14
医疗器械临床试验是医疗器械研发注册环节中至关重要的部分,同时,临床试验机构的数量变化在一定程度上也体现了当地医疗器械临床实验质量管理水平。 2017年11月发布的《医疗器械临床试验机构条件和备案管理办法》中明确规定医疗器械临床试验机构实行备案管理;在质量管理方面,2022年3月发布的《医疗器械临床试验质量……
国家药监局:集中带量采购中选医疗器械质量监管工作汇报会召开
2022-07-14
国家开会,抽检中选产品 7月12日,国家药监局召开集中带量采购中选医疗器械质量监管工作汇报会。 2家冠脉支架、4家人工关节集采中选企业汇报了集采中选产品、企业质量管理体系运行情况以及保障产品质量措施,天津市、山东省药监局就加强集采中选产品质量安全监管工作进行汇报。 ……
医疗器械临床试验目的如何设定?
2022-07-13
为贯彻落实中共中央办公厅、国务院办公厅《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》,加强医疗器械产品注册工作的管理,进一步提高注册审查质量,鼓励医疗器械研发创新,国家食品药品监督管理总局组织制定了医疗器械临床试验设计指导原则。 依据医疗器械临床试验设计指导原则的相关规定,临床试验需设定明……
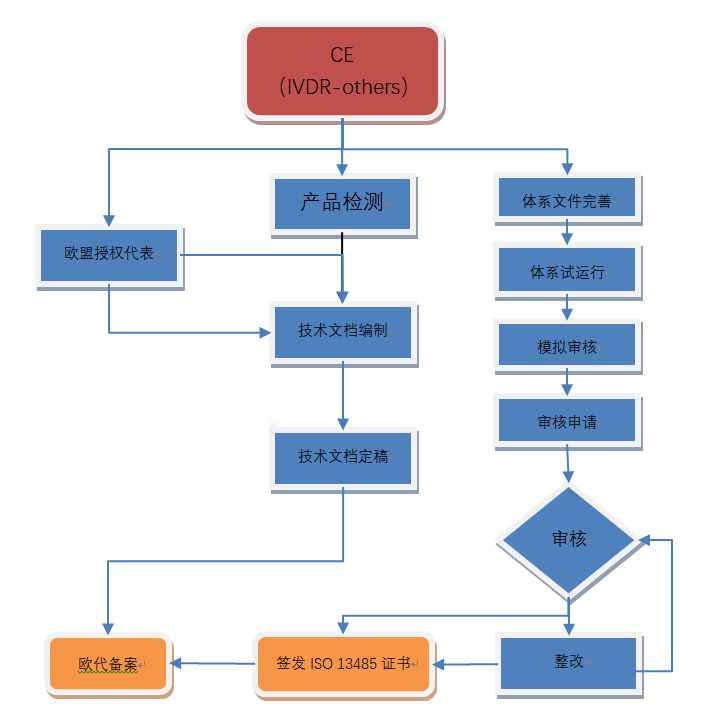
欧洲体外诊断(IVD)医疗器械CE标志
2022-07-12
在欧洲销售的所有体外诊断试剂(IVD)器械都需要CE标记。CE标记意味着IVD器械符合欧洲体外诊断器械指令(IVDD 98/79/EC),并且该器械可能在欧盟合法上市。欧洲新的体外诊断法规(IVDR)将于2022年强制实施,从而大大改变了IVD的监管要求。 根据IVDD指令,体外诊断器械在欧洲可分为四类: ……
在日本的医药品与医疗器械局(PMDA)医疗器械注册登记与审批
2022-07-12
由于复杂的注册登记流程和语言方面的障碍,日本一直被外国医疗器械制造商认为是挑战性比较高的市场之一。 但是一旦了解清楚其器械注册流程,您会发现它其实一点儿都不复杂,而且回报绝对物有所值。 日本利润丰厚的医疗器械市场依然是全世界第二大的市场,排在中国和德国之前。 日本的相关规定与审批流程 有兴趣在日本销售其产品……