2021年广东注册4729项第二类医疗器械全国第一
2022-08-12
广东省药品监督管理局(以下简称“广东省药品监管局”)始终坚持以习近平新时代中国特色社会主义思想为指导,全面落实党的十九大和十九届历次全会精神,认真落实习近平总书记“四个最严”要求,深入贯彻落实《关于全面加强药品监管能力建设的实施意见》,深化审评审批制度改革,持续推进监管创新,保障公众用械安全,促进医疗器械产业健康发展。……
《无源植入性骨、关节及口腔硬组织个性化增材制造医疗器械注册技术审查指导原则》导读
2022-08-11
二十世纪九十年代,我国已经开始了对于个性化医疗器械的探索和临床应用。2002年开始,定制式义齿的监管要求陆续出台。2015年,原国家食药监总局启动了定制式产品注册管理模式研究。2018年2月,器审中心发布了《定制式增材制造医疗器械注册技术审查指导原则(征求意见稿)》,首次向业界抛出了监管部门对于这类产品的技术思考,受到……
广药局:关于实施医疗器械主文档登记事项的通告
2022-08-11
为贯彻落实广东省药品监督管理局《关于优化第二类医疗器械注册审评审批的若干措施》的要求,进一步提高医疗器械审评审批质量,建立更加科学高效的审评审批体系,减少重复检验、重复评价,便利医疗器械生产企业选择原材料,简化注册申报,依据国家药品监督管理局《关于医疗器械主文档登记事项的公告》(2021年第36号)有关规定,现就实施第……
医疗器械临床试验的数据统计分析要点
2022-08-10
一、医疗器械临床试验的相关法规 临床试验是以受试人群(样本)为观察对象,观察试验器械在正常使用条件下作用于人体的效应或对人体疾病、健康状态的评价能力,以推断试验器械在预期使用人群(总体)中的效应。顾名思义,临床试验是证明产品安全性和有效性的重要途径和手段。 临床试验的成功需要严谨的试验设计,……
数字诊疗装备核心部件可靠性测试项目
2022-08-10
医疗器械行业急需社会化可靠性专业服务机构,解决医疗器械行业现有体制内检测机构可靠性服务功能的缺失和工程能力不足的问题。面向企业在产品研发过程提供可靠性技术服务,引导企业提出合理的可靠性要求,导入可靠性设计分析,对样机实施可靠性检测试验,开展使用期限分析与评价,确保新研器械最终能够符合注册检验和技术审评的要求,提升国产医……
医疗器械可用性工程所涉及的标准
2022-08-09
1、可用性工程在医疗器械中的应用 医学实践中越来越多地使用医疗器械诊断和治疗患者。医疗器械可用性不良引起的使用错误已成为人们日益关注可用性的原因。许多未采用可用性工程过程开发的医疗器械难以学习和使用,在医疗器械比较简单的时代,用户也许能应对不明确的、难以使用的用户接口;随着医疗卫生保健的发展,现在缺乏技能……
医疗器械临床试验前动物实验的考虑要点
2022-08-09
医疗器械临床前动物实验研究是许多Ⅲ类医疗器械,特别是创新型医疗器械进行临床试验研究之前需要开展的重要项目。医疗器械安全性和有效性评价中动物试验是重要手段之一。 医疗器械临床试验前动物实验研究,作为在临床试验之前初步验证医疗器械安全性及有效性的手段,对于尚没有大量临床应用历史的高风险医疗器械以及创新型医疗器……
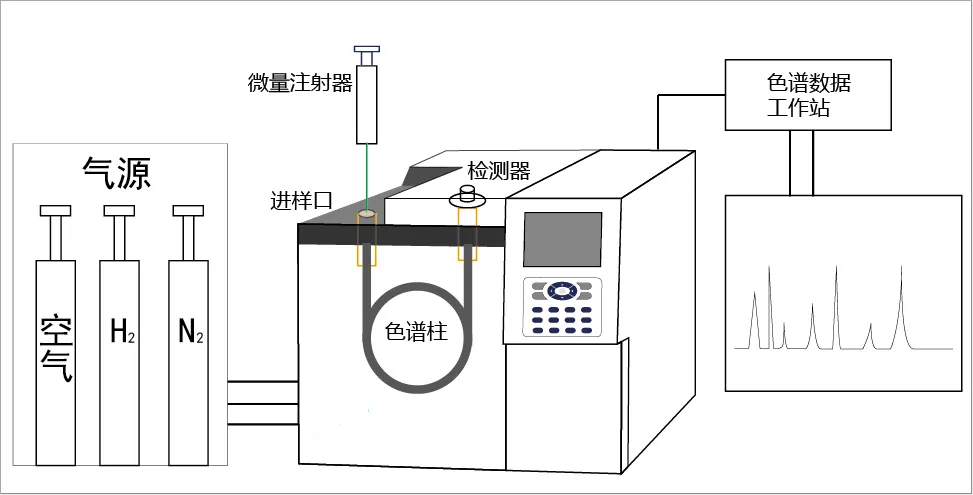
《医疗器械环氧乙烷残留量(气相色谱法)注册自检现场检查指南(试行)》征求意见
2022-08-06
为加强医疗器械注册管理,规范医疗器械注册自检现场核查工作,江苏省药监局核查中心组织研究起草了《江苏省医疗器械环氧乙烷残留量(气相色谱法)注册自检现场检查指南(试行)》(见附件),现向社会公开征求意见。请于2022年8月12日前,将意见和建议反馈我中心。意见反馈表请发送电子邮件至31491146@qq.com,邮件标题请……
植入性医疗器械产品的生产环境有何要求
2022-08-06
植入性医疗器械产品的放行检验有何要求? 对于自行具备产品灭菌能力的植入性医疗器械生产企业,其出厂检验项目规定对产品进行无菌检验,可按照规定执行;如规定检测生物指示剂(菌片),在对灭菌过程进行科学验证基础上,可采取检测菌片方式进行产品放行。 植入性医疗器械产品的生产环境有何要求? ……
消毒和灭菌的区别及微生物检测中常用的灭菌和消毒方法汇总
2022-08-05
消毒和灭菌两个词在实际使用中常被混用,其实它们的含义是有所不同的。消毒是指应用消毒剂等方法杀灭物体表面和内部的病原菌营养体的方法,而灭菌是指用物理和化学方法杀死物体表面和内部的所有微生物,使之呈无菌状态。 01物理方法 1、温度 利用温度进行灭菌、消毒或防腐,是……