医用空气压缩机组注册审查指导原则
2022-09-26
医用空气压缩机组注册审查指导原则 本指导原则是对医用空气压缩机组的一般要求,申请人应依据具体产品的特性确定其中内容是否适用。若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对注册申报资料的内容进行充实和细化。 本指导原则是供注册申请人和技术审评人员使用的指导性文件,但不包括注册……
高敏心肌肌钙蛋白检测试剂注册审查指导原则
2022-09-26
高敏心肌肌钙蛋白检测试剂注册审查指导原则 本指导原则旨在指导注册申请人对高敏心肌肌钙蛋白检测试剂注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。 本指导原则是针对高敏心肌肌钙蛋白检测试剂的一般要求,申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应……
一次性使用脑电电极注册审查指导原则
2022-09-24
一次性使用脑电电极注册审查指导原则 本指导原则旨在指导注册申请人对一次性使用脑电电极注册申报资料的准备及撰写,同时也为技术审评部门提供参考。 本指导原则是对一次性使用脑电电极的一般要求,申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对注……
糖化血红蛋白分析仪注册审查指导原则
2022-09-24
糖化血红蛋白分析仪注册审查指导原则 本指导原则旨在指导注册申请人(以下简称申请人)对糖化血红蛋白分析仪注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。 本指导原则是对糖化血红蛋白分析仪的一般要求,申请人应依据产品的具体特性确定其中内容是否适用。若不适用,需具体阐述理由及相应的……
前白蛋白检测试剂注册审查指导原则
2022-09-24
前白蛋白检测试剂注册审查指导原则 本指导原则旨在指导注册申请人对前白蛋白检测试剂注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。 本指导原则是对前白蛋白检测试剂的一般要求,申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具……
雌二醇检测试剂注册审查指导原则
2022-09-24
雌二醇检测试剂注册审查指导原则 本指导原则旨在指导注册申请人对雌二醇检测试剂注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。 本指导原则是对雌二醇检测试剂的一般要求,申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性……
疤痕修复材料产品注册审查指导原则
2022-09-23
疤痕修复材料产品注册审查指导原则 本指导原则旨在提供系统规范的指南性文件,用于指导注册申请人进行注册申报,同时也为技术审评部门提供技术指导。 本指导原则是对疤痕修复材料产品注册申报资料的一般要求,注册申请人应依据产品具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的……
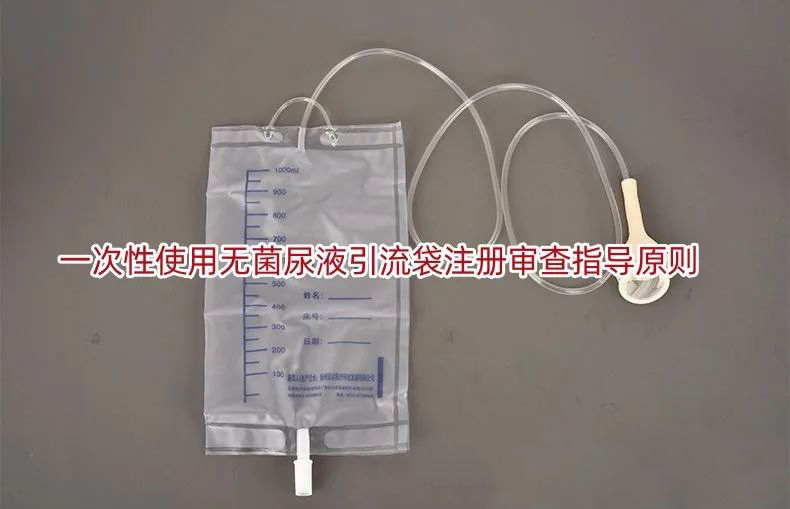
一次性使用无菌尿液引流袋注册审查指导原则
2022-09-23
一次性使用无菌尿液引流袋注册审查指导原则 本指导原则旨在指导注册申请人对一次性使用无菌尿液引流袋(以下简称:无菌尿液引流袋)注册申报资料的准备及撰写,同时也为技术审评部门审查注册申报资料提供参考。 本指导原则是对无菌尿液引流袋的一般要求,注册申请人应依据产品的具体特性确定其中内容是否适用。若不适用,……
电针治疗仪产品注册审查指导原则
2022-09-22
电针治疗仪产品注册审查指导原则 本指导原则旨在指导注册申请人对电针治疗仪产品注册申报资料的准备及撰写,同时也为技术审评部门提供参考。 本指导原则是对电针治疗仪产品的一般要求,申请人应依据产品的具体特性确定其中内容是否适用。若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对注册申报资料的……
一次性使用切口保护套产品注册审查指导原则
2022-09-22
一次性使用切口保护套产品注册审查指导原则 本指导原则旨在指导注册申请人对一次性使用切口保护套产品注册申报资料的准备及撰写,同时也为技术审评部门提供参考。 本指导原则是对一次性使用切口保护套产品的一般要求,申请人应依据产品的具体特性确定其中内容是否适用。若不适用,需具体阐述理由及相应的科学依据,并依据……
纤维蛋白单体测定试剂注册审查指导原则
2022-09-21
纤维蛋白单体测定试剂注册审查指导原则 本指导原则旨在指导注册申请人对纤维蛋白单体测定试剂注册申报资料的准备及撰写,同时也为技术审评部门提供参考。 本指导原则是对纤维蛋白单体测定试剂的一般要求,申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特……
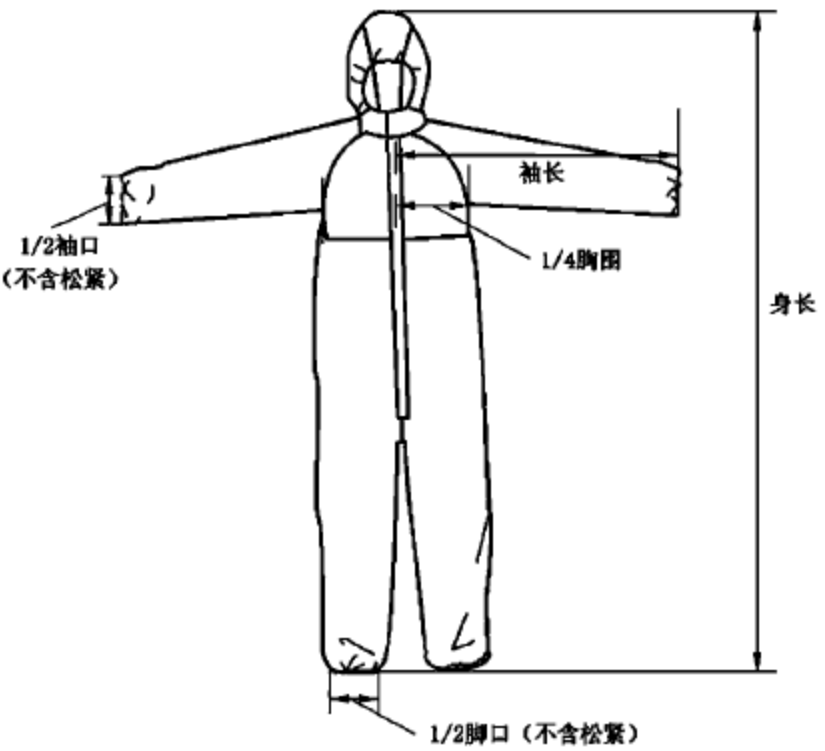
医用防护服产品注册审查指导原则
2022-09-21
医用防护服产品注册审查指导原则 本指导原则旨在指导注册申请人准备及撰写医用防护服产品注册申报资料,同时也为技术审评部门审查注册申报资料提供参考。 本指导原则是对医用防护服产品的一般要求,注册申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性……