
日本医疗器械一般名称数据库探析
发布人:管理员 发布时间:2022-06-21
张春青1#,周良彬2#,王越1 (1. 中国食品药品检定研究院,北京 100050;2. 广东省医疗器械质 量监督检验所,广州 510663)
摘要 目的:探讨日本医疗器械监管数据库建设与分类命名工作思路,为我国医疗器械监管信息化建设提供技术支撑。
方法:解析日本医疗器械一般名称(JMDN)数据库结构层级,分析其分类命名信息。 结果与结论:数据库的建立与管理体现了日本医疗器械的监管立足于本国实际,保持与国际监管思路的 良好接轨,注重法规的长期稳定性和实际可操作性的工作思路,对进一步完善我国医疗器械信息化建设 具有重要借鉴意义。
关键词: 医疗器械;通用名称;术语;数据库 中图分类号: R95 文献标识码:A 文章编号:1002-7777(2020)01-0108-06 doi:10.16153/j.1002-7777.2020.01.017 Analysis and Discussion on the Japanese Medical Device Nomenclature (JMDN) Database Zhang Chunqing1#, Zhou Liangbin2#, Wang Yue1 (1. National Institutes for Food and Drug Control, Beijing 100050, China; 2. Guangdong Medical Devices Quality Surveillance and Test Institute, Guangzhou 510663, China) Abstract Objective: To discuss the construction, classification and nomenclature of medical device regulatory databases in Japan in order to provide technical support for the construction of medical device regulation informationization in China. Methods: The structure, classification and nomenclature of Japanese medical device nomenclature (JMDN) databases were analyzed. Results and Conclusion: The establishment and management of the JMDN databases have reflected the facts that the medical device supervision in Japan is linked to the actual situation of the country, and the idea keeps in line with the international regulations and pays attention to the longterm stability and practical operability of the regulations, all of which will provide an important reference for further improving the construction of medical device regulation informationization in China.
Keywords: medical devices; general names; nomenclature; database
2004年,日本厚生劳动省以通告的形式[1]公布 了日本医疗器械一般名称( Japanese Medical Device Nomenclature,JMDN)数据库,它以当时全球医 疗器械术语(Global Medical Device Nomenclature, GMDN)数据库的命名术语体系和全球医疗器械法规协调工作组(Global Harmonization Task Force, GHTF)医疗器械分类规则为基础,基于日本监管 实际需求而制定,是公开且要求强制执行的文件。 制造商不仅在注册时需要提供产品对应的JMDN数 据库信息,而且需要在产品标签和随机文件中标明产品的一般名称和代码、类别名称及代码。可见 JMDN数据库在日本医疗器械的基础地位与作用。
日本独立行政法人医药品及医疗器械综合 管理机构(Pharmaceuticals And Medical Devices Agency,PMDA)是厚生劳动省下独立管理机构、 独立行政法人, 医疗器械安全和有效性评估是其 重要职能之一。近年来,日本对贸易全球化形势越 来越重视,在医疗器械领域逐步推动标准、法规 等文件英文版本的转化发布,PMDA官网上发布的 JMDN数据库,向公众免费提供完整版[2](日文版 本)和简化版 [3](英文版本)下载查询服务。
本文基于PMDA官网提供的JMDN数据库[2]信 息,对其数据库构建思路以及包含的日本医疗器 械分类命名信息进行分析,为相关法规研究提供 参考信息。需要说明的是,PMDA官方网站发布的 JMDN数据库,未包括体外诊断试剂产品,笔者也未在PMDA官网发现可供查询或下载的该类产品一
般名称数据库,但有日文版的体外诊断用医药品类
产品信息数据库可以查询日本体外诊断试剂产品部分信息。
1 JMDN数据库的基础信息和框架解析
1.1 JMDN数据库信息概况
通过PMDA官方网站下载获得的JMDN
数据库英文版本包括以下内容:一般名称
(Japanese Medical Device Nomenclature)、定义
(Definition)、JMDN代码(JMDN Code)、分类
(Classification)、规则(Rule)。其日文版本内
容则更加丰富,除了以上内容之外,还列出了类别
代码、类别名称、管理基本要求以及相关管理文件
索引信息。
JMDN数据库中收录产品共6大类105项4349
条,见表1。
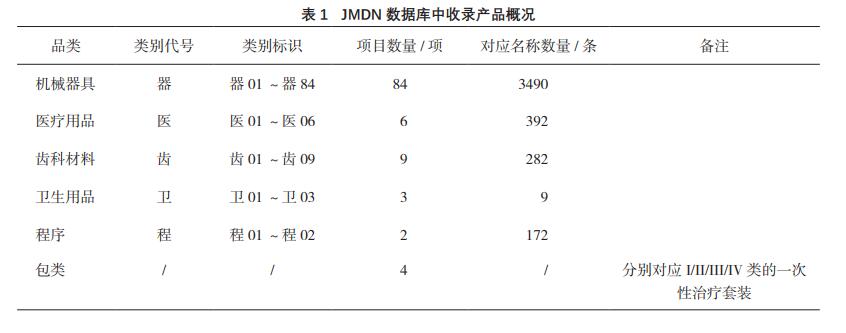
通过表1的层级划分,JMDN数据库建立了从
粗到细,最终落实于一般名称的层级结构,便于使
用者掌握查询。
JMDN数据库在整体发布之后,根据监管需要
和行业产品发展[敏感词]状况,采取公开发布变更文件
的形式对个别条目内容进行调整,数据库随后会根
据公告内容进行更新。通过统计JMDN数据库中各
词条的更新信息发现,自2004年JMDN数据库发布
至今,共对442个词条进行了更改、追加,未发生
更新词条3907条,占比达90%,体现出日本医疗器
械监管保持了长期的一致性。
PMDA官网上可下载的JMDN数据库完整版(日文),可根据[敏感词]发布的补充修改文件及时更
新,而简化版(英文)的更新则相对延迟。此外,
使用者还可直接下载JMDN数据库的Excel或PDF完
整版本,也可以通过在搜索界面输入名称、定义、
代码、分类等信息,对数据库相关项目进行检索。
1.2 JMDN数据库框架解析
JMDN数据库的核心是一般名称,源于当时的
GMDN数据库的优先术语(Preferred Term,简称
PT)。GMDN不仅为医疗器械监管提供技术支持,
还用于医疗机构的库存管理,所以GMDN数据库中
产品范围通常比医疗器械的管理范围要大,包括一
些非医疗器械的临床机构用品,而各国根据实际情况,对医疗器械的管理范围也不完全一致。日本在
制定JMDN数据库时,根据本国监管实际对其中品
种(优先术语)进行了筛选,剔除了不符合本国监
管思路的品种,并根据监管分类的需要,对选择的
品种进一步细化拆分,最终确定了相应的一般名称
和代码。
JMDN数据库在GMDN数据库原有的五位数字
代码的基础上新增了三位数字的后缀,作为细化
品种的代码区(如果直接采用GMDN数据库的PT,
则末三位为000),形成JMDN数据库的8位数字代
码,同时明确各个一般名称的管理分类及其所依据
的GHTF分类规则。此外,日本根据本国监管实际
需要起草JMDN数据库文件时,增列了GMDN数据
库(2003年版本)当时没有收纳器械的一般名称,
这类产品在数据库中代码首位为7(来自GMDN词
条的代码首位为1、3或4)。
利用新增的三位数字代码对名称进行分割
时,个位数字体现管理类别的差异,十位则为管理
类别不变时体现其他特性的划分(体现的特性因产
品类型不同有所区别),百位体现产品是否含有药
物、生物制品等方面特点,逻辑顺序依次为从个
位→十位→百位的特征进行划分。数位上数字为
“0”时,指未作该类特征分割,非“0”数字的含
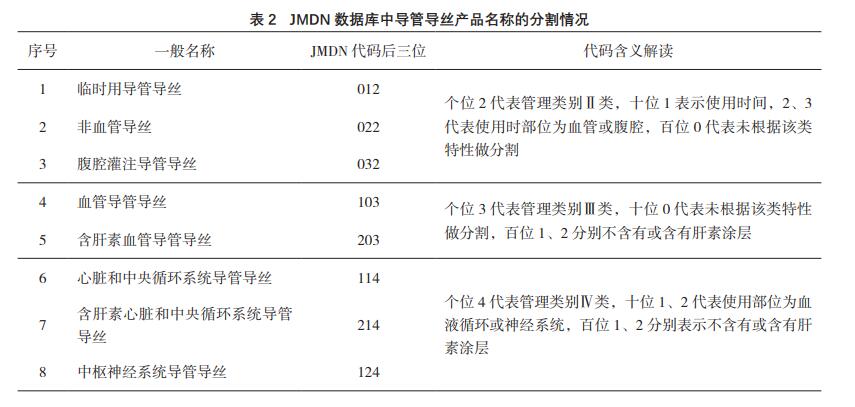
义根据产品情况各有不同。例如根据使用时间、使
用部位、是否含有药品生物制品的特点,原GMDN
数据库词条“35094导管导丝”在JMDN数据库中分
割为8个一般名称(见表2,表中产品JMDN代码前
五位均为35094)。如表2所示,利用三位数字进行
名称分割时,首先根据产品管理分类(Ⅱ/Ⅲ/Ⅳ)
将导管导丝产品分成三大类,然后在此基础上进一
步进行十位特征、百位特征的划分。
2 JMDN数据库中命名和分类数据分析
2.1 医疗器械命名信息统计分析
JMDN数据库作为服务于医疗监管的命名与分
类信息系统,其发展过程注重维持监管要求的一致
性和长期稳定性。如前所述,在引用GMDN数据库
术语系统作为其命名体系基础的前提下,JMDN数
据库对体系进行本土化设计与重建,对GMDN数据
库中的术语进行剔除和细分,并加入新的词条。
GMDN数据库根据全球生产企业的要求对名称进行删除、修改、新增,根据情况即时更新相关内容,
本文采用的数据即为2019年5月23日更新的JMDN
数据库信息,它直接采用GMDN数据库(首位代码
1、3或4,代码末三位为000)的词条有2033条,占
比47%;在GMDN数据库词条基础上进行细化的词
条(首位代码1、3或4,且末三位不是000)有1094
条,占比25%;日本自主起草的词条(首位为7)
有1222条,占比28%。
以GMDN数据库为基础建立JMDN数据库体系之后,厚生劳动省并没有把JMDN数据库与GMDN
数据库保持一致作为JMDN数据库体系建设和维护
重点考虑的内容,而是着重于保持日本监管要求的
稳定性。GMDN数据库不断更新,JMDN数据库强
调稳定,两个数据库虽然框架基本相同,但具体条
目的一致程度在逐渐减弱。以上信息体现出JMDN
数据库命名工作以GMDN数据库为基础,结合本国
监管实际进行细化和调整的根本思路。
2.2 医疗器械分类信息统计分析
JMDN数据库在引用GMDN数据库词条命名系
统及定义的基础上,对其所定义产品的管理类别及
所引分类规则进行了明确。JMDN数据库涉及医疗
器械命名、定义、代码、分类等信息,是比GMDN
数据库的内容更加丰富的综合信息系统。因此,
JMDN数据库也是医疗器械分类管理体系中的一项
基础性文件。
JMDN数据库中的产品管理分类,Ⅰ类产品
1205条,Ⅱ类产品1983条,Ⅲ类产品796条,Ⅳ产
品365条,占比依次为28%、46%、18%、8%。笔者将JMDN数据库的管理分类数据与数据库制定之
前的管理类别情况进行对比分析,结果显示,新
旧管理类别一致的词条1559条,新确定(之前未对
词条品种明确类别)的词条1978条,升类(包括
Ⅰ升Ⅱ,或Ⅰ/Ⅱ升Ⅲ之类情况)的词条469条,降
类的词条95条,统一管理类别(即从多个管理类
别中选择一个,如Ⅰ/Ⅱ统一为Ⅰ)词条248条。此
外,JMDN数据库中,对代码末三位进行划分的情
况共105种(001、012、103、213等),涉及词条
1370条,其中仅因为管理类别差异进行划分的情况
共4种(001、002、003、004),对应词条606条,
占比44%。以上数据说明在JMDN数据库制定过程
中,管理类别的确定、调整以及因为管理类别差异
进行的词条细分等管理类别分类相关工作占了相当
大的工作量。
JMDN数据库用以确定产品管理类别的分类规
则思路和体系,基本上与GHTF的分类规则保持一
致。在JMDN数据库中,列出了每个一般名称词条的
管理分类以及对应的分类规则号,对应情况见表3。
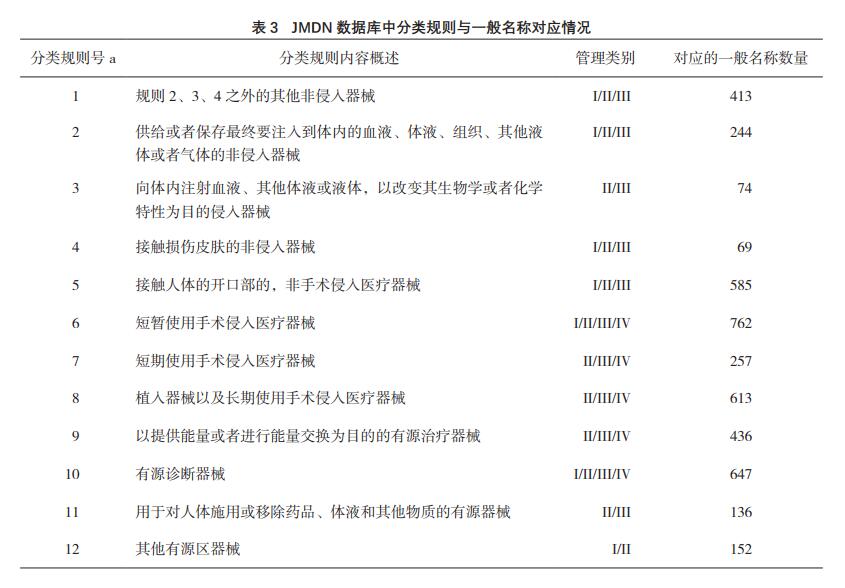
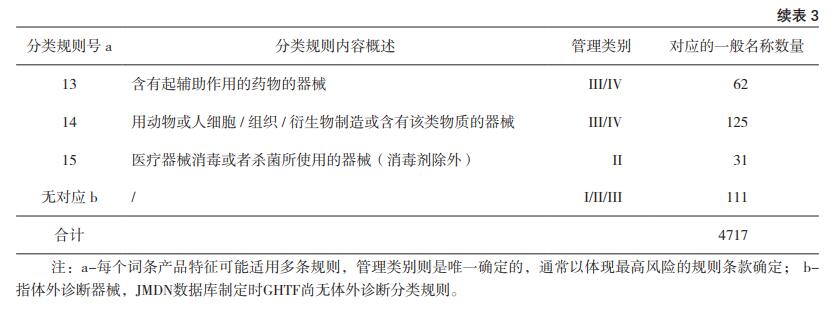
表3中一般名称词条总数为4717条,超过JMDN
数据库的词条总数(4349条)。这是因为JMDN数
据库中存在353条适用于两条及以上规则或子条
款的词条。例如牙科电动旋转动力装置(Code:
70690000),其定义为“一种牙科电动设备,用于
切割/抛光牙齿、假牙、牙冠等。不包括牙科电动
手机。可能包括用于从口腔剥离/移除假体、异物
等物体的器械”,因而其既适用5-⑥(接触人体
的开口部的,非手术侵入医疗器械),也适用规则
9(以提供能量为目的的有源治疗器械)。
通过将一般名称与管理类别、分类规则进行
一一对应,将日本医疗器械分类系统与国际体系进
行了对应关联,极大地便利了使用者对产品分类
要求和思路的理解和掌握。值得注意的是,GHTF
在2008年发布了7条体外诊断器械分类规则[4],其
医疗器械分类原则也在2012年修订发布[5],分类规
则数更新至17条,但JMDN数据库并未针对这些变
化更新自己的体系,仍然保持原有分类体系。由于
GHTF医疗器械分类规则更新幅度较小,前后基本
思路保持一致,JMDN数据库仍然能够很好地衔接
本国监管思路与国际分类体系。
3 与其他数据库的关联
PMDA官网对JMDN数据库检索的结果以
一般名称为基本单位显示,除了JMDN数据库
文件的内容外,还有一项“基准”(Criteria in
Regulation),可以关联到该产品对应的认证基准/
承认基准/审查指导原则(如有),里面列出了同
样适用于该“基准”的产品一般名称信息以及适用
的法规和标准。这一基准数据库[6]的搜索界面和结
果可以在日文和英文之间转换,可输入的检索项目有基准的名称、一般名称、预期用途等。截至2019
年7月19日,日本厚生省制定了945个认证基准、44
个承认基准和9个审查指导原则,但并未实现所有
一般名称的覆盖,仍然有相当一部分一般名称无法
搜索到对应的基准信息。
除了JMDN数据库之外,日本也有产品信息数
据库[7]等其他数据库,提供产品的制造商、说明
书、不良事件等方面信息的检索,但仅有日文版
本,可输入的检索项目有一般名称及类别名称、商
品名、制造商名称、审批号、预期用途等等。产品
信息数据库中各大类对应的检索结果分别为机械
器具,25802项;医疗用品,3714项;齿科材料,
820项;卫生用品,12项;程序,92项;总计30440
项。JMDN数据库的“空栏”项目(包类)下I/II/
III/IV类的一次性治疗套装四个一般名称在该数据
库中并无对应信息,可见这部分一般名称的用途与
该数据库无关。
4 分析与结论
本文通过对JMDN数据库不同层面信息及数
据的汇总分析,揭示了JMDN数据库的整体工作思路。
一是JMDN数据库在接轨国际的同时,注重保
持监管要求的长期稳定性。JMDN数据库以国际上
较大范围内通用的GHTF分类规则体系、GMDN数
据库术语系统为基础,较好地保证了JMDN数据库
系统与国际监管思路的协调互通。虽然JMDN数据
库建立之后并未随着GMDN数据库/GHTF文件的更
新而调整,但其整体框架类似,推出的英文简版
数据库为有效的信息沟通提供了保证。JMDN数据
库建立之初,联系本国实际在词条方面进行重新划分,有相当大比例的自主起草内容,能够有效满足
本国监管需要。
二是逻辑关系明确,便于产品的定位查询。
JMDN数据库要素和结构方面的信息表明,JMDN数
据库通过建立从大到小的类别划分思路,体现出数
据库较强的逻辑层级关系,便于产品的定位查询。
三是医疗器械命名和医疗器械分类管理体系
紧密结合。JMDN数据库制定过程中,将医疗器械
分类管理体系与命名系统有机结合,建立了“医疗
器械一般名称+管理类别+分类规则”紧密结合的
数据库结构模式,方便从业者快速、准确地掌握各
个词条对应的管理类别以及所依据的分类规则,有
力地呼应与支持了日本医疗器械监管统一使用一
般名称、以分类规则指导医疗器械分类的整体管
理思路。
四是JMDN数据库与外部数据库有效关联。
JMDN数据库通过与基准、产品信息数据库进行网
络或逻辑上的关联,充分发挥一般名称、类别等监
管层级概念的基础作用,便于使用者更系统地获取
产品扩展信息。
综上所述,JMDN数据库的系统注重与国际接
轨,又能体现本国特色的数据库建设思路,数据库
“命名+分类+分类规则”的形式,充分体现了医
疗器械分类、命名互为支持并为医疗器械监管提供
很好的技术支撑,为当前我国医疗器械行业信息化
建设提供了现实的借鉴。
参考文献:
[1] 日本厚生劳动省. 药食发第0720022号 医薬品、医療機
器等の品質、有効性及び安全性の確保等に関する法
律第二条第五項から第七項までの規定により厚生労
働大臣が指定する高度管理医療機器、管理医療機器
及び一般医療機器(告示)及び医薬品、医療機器等の
品質、有効性及び安全性の確保等に関する法律第二
条第八項の規定により厚生労働大臣が指定する特定
保守管理医療機器(告示)の施行について[S]. 2004.
[2] Pharmaceuticals and Medical Devices Agency. 一般的名称
検索[EB/OL]. (2019-06-28)[2019-09-10]. http://www.
std.pmda.go.jp/stdDB/index.html.
[3] GMDN Agency. Global Medical Device Nomenclature
[EB/OL].(2019-07-11)[2019-09-10].https://www.
gmdnagency.org/Terms/Search.
[4] The Global Harmonization Task Force. Principles of IVD
Medical Devices Classification[S]. 2008.
[5] The Global Harmonization Task Force. Principles of Medical
Devices Classification[S]. 2012.
[6] Pharmaceuticals and Medical Devices Agency. 認証/承認
基準等検索 [EB/OL].(2019-06-28)[2019-09-10].
http://www.std.pmda.go.jp/stdDB/index.html.
[7] Pharmaceuticals and Medical Devices Agency. 医療機器
情報検索 [EB/OL].(2019-07-11)[2019-09-10]. http://
www.pmda.go.jp/PmdaSearch/kikiSearch/.



